Termodinamika është një degë e rëndësishme e fizikës. Mund të themi me siguri se arritjet e tij kanë çuar në shfaqjen e epokës teknologjike dhe kanë përcaktuar kryesisht rrjedhën e historisë njerëzore gjatë 300 viteve të fundit. Artikulli diskuton ligjet e parë, të dytë dhe të tretë të termodinamikës dhe zbatimin e tyre në praktikë.
Çfarë është termodinamika?
Para se të formulojmë ligjet e termodinamikës, le të kuptojmë se çfarë bën ky seksion i fizikës.
Fjala "termodinamikë" është me origjinë greke dhe do të thotë "lëvizje për shkak të nxehtësisë". Kjo do të thotë, kjo degë e fizikës është e angazhuar në studimin e çdo procesi, si rezultat i të cilave energjia termike shndërrohet në lëvizje mekanike dhe anasjelltas.
Ligjet bazë të termodinamikës u formuluan në mesin e shekullit të 19-të. Shkenca e "lëvizjes dhe nxehtësisë" e konsideron sjelljen e të gjithë sistemit në tërësi, duke studiuar ndryshimin në parametrat e tij makroskopikë - temperaturën, presionin dhe vëllimin, dhe duke mos i kushtuar vëmendje strukturës së tij mikroskopike. Për më tepër, i pari prej tyre luan një rol themelor në formulimin e ligjevetermodinamika në fizikë. Është kurioze të theksohet se ato janë nxjerrë vetëm nga vëzhgimet eksperimentale.
Koncepti i një sistemi termodinamik

Do të thotë çdo grup atomesh, molekulash ose elementësh të tjerë që konsiderohen si një e tërë. Të tre ligjet janë formuluar për të ashtuquajturin sistem termodinamik. Shembuj janë: atmosfera e Tokës, çdo organizëm i gjallë, përzierja e gazit në një motor me djegie të brendshme, etj.
Të gjitha sistemet në termodinamikë i përkasin një prej tre llojeve:
- Hapur. Ata shkëmbejnë si nxehtësinë ashtu edhe lëndën me mjedisin. Për shembull, nëse ushqimi gatuhet në një tenxhere në zjarr të hapur, atëherë ky është një shembull i gjallë i një sistemi të hapur, pasi tenxherja merr energji nga mjedisi i jashtëm (zjarri), ndërsa vetë rrezaton energji në formën e nxehtësisë, dhe uji gjithashtu avullohet prej tij (metabolizmi).
- Mbyllur. Në sisteme të tilla nuk ka shkëmbim të materies me mjedisin, megjithëse ndodh shkëmbimi i energjisë. Kthimi në rastin e mëparshëm: nëse e mbuloni kazanin me kapak, mund të merrni një sistem të mbyllur.
- I izoluar. Ky është një lloj sistemesh termodinamike që nuk shkëmbejnë materie ose energji me hapësirën përreth. Një shembull do të ishte një termos që përmban çaj të nxehtë.
Temperatura termodinamike

Ky koncept nënkupton energjinë kinetike të grimcave që formojnë trupat përreth, e cila pasqyron shpejtësinëlëvizje të rastësishme të grimcave. Sa më i madh të jetë, aq më e lartë është temperatura. Prandaj, duke reduktuar energjinë kinetike të sistemit, ne e ftohim atë.
Ky koncept nënkupton energjinë kinetike të grimcave që formojnë trupat përreth, e cila pasqyron shpejtësinë e lëvizjes kaotike të grimcave. Sa më i madh të jetë, aq më e lartë është temperatura. Prandaj, duke reduktuar energjinë kinetike të sistemit, ne e ftohim atë.
Temperatura termodinamike shprehet në SI (Sistemi Ndërkombëtar i Njësive) në Kelvin (për nder të shkencëtarit britanik William Kelvin, i cili i pari propozoi këtë shkallë). Kuptimi i ligjit të parë, të dytë dhe të tretë të termodinamikës është i pamundur pa një përkufizim të temperaturës.
Një ndarje e një shkalle në shkallën Kelvin gjithashtu korrespondon me një shkallë Celsius. Shndërrimi ndërmjet këtyre njësive kryhet sipas formulës: TK =TC + 273, 15, ku TK dhe TC - temperaturat në kelvin dhe gradë Celsius respektivisht.
E veçanta e shkallës Kelvin është se ajo nuk ka vlera negative. Zero në të (TC=-273, 15 oC) korrespondon me gjendjen kur lëvizja termike e grimcave të sistemit mungon plotësisht, ato duket se janë "të ngrira".
Ruajtja e energjisë dhe ligji i parë i termodinamikës

Në 1824, Nicolas Léonard Sadi Carnot, një inxhinier dhe fizikant francez, bëri një sugjerim të guximshëm që jo vetëm çoi në zhvillimin e fizikës, por gjithashtu u bë një hap i madh në përmirësimin e teknologjisë. E tijmund të formulohet si më poshtë: "Energjia nuk mund të krijohet apo shkatërrohet, ajo mund të transferohet vetëm nga një gjendje në tjetrën."
Në fakt, fraza e Sadi Carnot postulon ligjin e ruajtjes së energjisë, i cili formoi bazën e ligjit të parë të termodinamikës: "Sa herë që një sistem merr energji nga jashtë, ai e shndërron atë në forma të tjera, kryesore e të cilat janë termike dhe mekanike."
Formula matematikore për ligjin e parë është shkruar si më poshtë:
Q=ΔU + A, këtu Q është sasia e nxehtësisë së transferuar nga mjedisi në sistem, ΔU është ndryshimi në energjinë e brendshme të këtij sistemi, A është puna e përsosur mekanike.
Proceset adiabatike
Një shembull i mirë i tyre është lëvizja e masave ajrore përgjatë shpateve malore. Masa të tilla janë të mëdha (kilometra ose më shumë), dhe ajri është një izolues i shkëlqyer i nxehtësisë. Vetitë e vërejtura na lejojnë të konsiderojmë çdo proces me masa ajrore që ndodhin brenda një kohe të shkurtër si adiabatike. Kur ajri ngrihet në një shpat mali, presioni i tij bie, ai zgjerohet, domethënë kryen punë mekanike dhe, si rezultat, ftohet. Përkundrazi, lëvizja në rënie e masës ajrore shoqërohet me rritje të presionit në të, ajo ngjesh dhe për këtë shkak nxehet shumë.
Zbatimi i ligjit të termodinamikës, i cili u diskutua në nëntitullin e mëparshëm, demonstrohet më lehtë duke përdorur shembullin e një procesi adiabatik.
Sipas përkufizimit, si rezultat i tij nuk ka shkëmbim të energjisë memjedisi, pra në ekuacionin e mësipërm, Q=0. Kjo çon në shprehjen e mëposhtme: ΔU=-A. Shenja minus këtu do të thotë që sistemi kryen punë mekanike duke reduktuar energjinë e tij të brendshme. Duhet të kujtojmë se energjia e brendshme varet drejtpërdrejt nga temperatura e sistemit.
Drejtimi i proceseve termike
Kjo çështje merret me ligjin e dytë të termodinamikës. Me siguri të gjithë e vunë re se nëse sillni në kontakt dy objekte me temperatura të ndryshme, atëherë i ftohti gjithmonë do të nxehet, dhe ai i nxehtë do të ftohet. Vini re se procesi i kundërt mund të ndodhë brenda kornizës së ligjit të parë të termodinamikës, por ai nuk zbatohet kurrë në praktikë.
Arsyeja e pakthyeshmërisë së këtij procesi (dhe të gjitha proceseve të njohura në Univers) është kalimi i sistemit në një gjendje më të mundshme. Në shembullin e konsideruar me kontaktin e dy trupave me temperatura të ndryshme, gjendja më e mundshme do të jetë ajo në të cilën të gjitha grimcat e sistemit do të kenë të njëjtën energji kinetike.
Ligji i dytë i termodinamikës mund të formulohet si më poshtë: "Nxehtësia nuk mund të transferohet kurrë spontanisht nga një trup i ftohtë në një trup të nxehtë." Nëse e prezantojmë konceptin e entropisë si masë e çrregullimit, atëherë ai mund të përfaqësohet si më poshtë: "Çdo proces termodinamik vazhdon me një rritje të entropisë".
Motor ngrohje

Ky term kuptohet si një sistem që, për shkak të furnizimit të tij me energji të jashtme, mund të kryejë punë mekanike. Së parimotorët me nxehtësi ishin motorë me avull dhe u shpikën në fund të shekullit të 17-të.
Ligji i dytë i termodinamikës luan një rol vendimtar në përcaktimin e efektivitetit të tyre. Sadi Carnot vërtetoi gjithashtu se efikasiteti maksimal i kësaj pajisjeje është: Efikasiteti=(T2 - T1)/T2, këtu T2 dhe T1 janë temperaturat e ngrohësit dhe të frigoriferit. Puna mekanike mund të bëhet vetëm kur ka një rrjedhje të nxehtësisë nga një trup i nxehtë në një të ftohtë dhe kjo rrjedhë nuk mund të shndërrohet 100% në energji të dobishme.
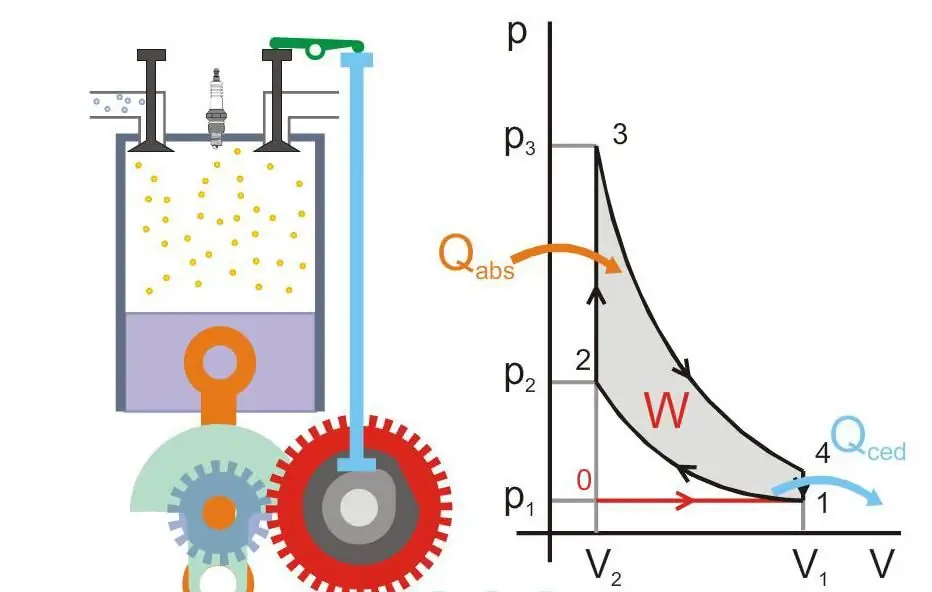
Figura më poshtë tregon parimin e funksionimit të një motori me ngrohje (Qabs - nxehtësia e transferuar në makinë, Qced - humbja e nxehtësisë, W - punë e dobishme, P dhe V - presioni dhe vëllimi i gazit në piston).
Zero absolute dhe postulati i Nernst
Më në fund, le të kalojmë në shqyrtimin e ligjit të tretë të termodinamikës. Quhet edhe postulati Nernst (emri i fizikanit gjerman që e formuloi për herë të parë në fillim të shekullit të 20-të). Ligji thotë: “Zoja absolute nuk mund të arrihet me një numër të kufizuar procesesh”. Kjo do të thotë, është e pamundur në asnjë mënyrë që të "ngrihen" plotësisht molekulat dhe atomet e një lënde. Arsyeja për këtë është shkëmbimi i vazhdueshëm ekzistues i nxehtësisë me mjedisin.

Një përfundim i dobishëm i nxjerrë nga ligji i tretë i termodinamikës është se entropia zvogëlohet ndërsa njeriu lëviz drejt zeros absolute. Kjo do të thotë se sistemi tenton të organizohet vetë. Ky fakt mundpërdorni, për shembull, për të transferuar paramagnetët në një gjendje ferromagnetike kur ftohen.
Është interesante të theksohet se temperatura më e ulët që është arritur deri më tani është 5·10−10 K (2003, laborator MIT, SHBA).






