Kapaciteti i nxehtësisë i një gazi është sasia e energjisë që një trup thith kur nxehet me një shkallë. Le të analizojmë karakteristikat kryesore të kësaj sasie fizike.

Përkufizime
Nxehtësia specifike e një gazi është masa njësi e një substance të caktuar. Njësitë e tij matëse janë J/(kg·K). Sasia e nxehtësisë që përthithet nga trupi në procesin e ndryshimit të gjendjes së tij të grumbullimit lidhet jo vetëm me gjendjen fillestare dhe përfundimtare, por edhe me metodën e kalimit.

Departament
Kapaciteti i nxehtësisë i gazrave ndahet me vlerën e përcaktuar në vëllim konstant (Cv), presion konstant (Cр).
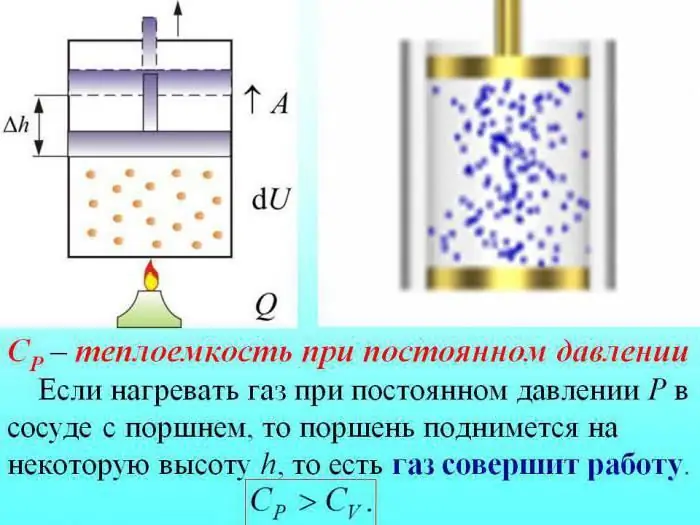
Në rastin e ngrohjes pa ndryshuar presionin, një pjesë e nxehtësisë shpenzohet për të prodhuar punën e zgjerimit të gazit, dhe një pjesë e energjisë shpenzohet për të rritur energjinë e brendshme.
Kapaciteti i nxehtësisë së gazeve në presion konstant përcaktohet nga sasia e nxehtësisë që shpenzohet për rritjen e energjisë së brendshme.
Gjendja e gazit: veçoritë, përshkrimi
Kapaciteti i nxehtësisë i një gazi ideal përcaktohet duke marrë parasysh faktin se Сp-Сv=R. Sasia e fundit quhet konstanta e gazit universal. Vlera e saj korrespondon me 8,314 J/(mol K).
Kur kryeni llogaritjet teorike të kapacitetit të nxehtësisë, për shembull, kur përshkruani marrëdhënien me temperaturën, nuk mjafton të përdorni vetëm metoda termodinamike, është e rëndësishme të armatoseni me elementë të fizikës statike.
Kapaciteti termik i gazeve përfshin llogaritjen e vlerës mesatare të energjisë së lëvizjes përkthimore të disa molekulave. Një lëvizje e tillë përmblidhet nga lëvizja rrotulluese dhe përkthimore e molekulës, si dhe nga dridhjet e brendshme të atomeve.
Në fizikën statike, ka informacion që për çdo shkallë të lirisë së lëvizjes rrotulluese dhe përkthimore, ekziston një sasi për një gaz që është e barabartë me gjysmën e konstantës së gazit universal.

Fakte interesante
Një grimcë e një gazi monoatomik supozohet të ketë tre shkallë lirie përkthimore, kështu që nxehtësia specifike e një gazi ka tre shkallë lirie përkthimore, dy rrotulluese dhe një vibruese. Ligji i shpërndarjes së tyre uniforme çon në barazimin e nxehtësisë specifike në një vëllim konstant me R.
Gjatë eksperimenteve, u zbulua se kapaciteti i nxehtësisë së një gazi diatomik korrespondon me vlerën R. Një mospërputhje e tillë midis teorisë dhe praktikës shpjegohet me faktin se kapaciteti i nxehtësisë së një gazi ideal lidhet me kuantike efektet, prandaj, kur bëni llogaritjet, është e rëndësishme të përdorni statistika të bazuara në kuantikemekanika.
Bazuar në themelet e mekanikës kuantike, çdo sistem grimcash që lëkunden ose rrotullohen, duke përfshirë molekulat e gazit, ka vetëm disa vlera diskrete të energjisë.
Nëse energjia e lëvizjes termike në sistem nuk është e mjaftueshme për të ngacmuar lëkundjet e një frekuence të caktuar, lëvizje të tilla nuk kontribuojnë në kapacitetin total të nxehtësisë së sistemit.
Si rezultat, një shkallë specifike lirie bëhet "e ngrirë", është e pamundur të zbatohet ligji i barazisë ndaj saj.
Kapaciteti termik i gazeve është një karakteristikë e rëndësishme e gjendjes nga e cila varet funksionimi i të gjithë sistemit termodinamik.
Temperatura në të cilën ligji i barazisë mund të zbatohet në shkallën vibruese ose rrotulluese të lirisë karakterizohet nga teoria kuantike, lidh konstantën e Plankut me konstanten Boltzmann.

Gaze diatomike
Hapësirat midis niveleve të energjisë rrotulluese të gazrave të tillë janë një numër i vogël gradësh. Përjashtim bën hidrogjeni, në të cilin vlera e temperaturës përcaktohet me qindra gradë.
Kjo është arsyeja pse kapaciteti i nxehtësisë i një gazi në presion konstant është i vështirë të përshkruhet me ligjin e shpërndarjes uniforme. Në statistikat kuantike, gjatë përcaktimit të kapacitetit të nxehtësisë, merret parasysh se pjesa vibruese e saj, në rastin e uljes së temperaturës zvogëlohet shpejt dhe arrin zero.
Ky fenomen shpjegon faktin se në temperaturën e dhomës praktikisht nuk ka asnjë pjesë vibruese të kapacitetit të nxehtësisë, përgaz diatomik, korrespondon me konstanten R.
Kapaciteti i nxehtësisë i një gazi në vëllim konstant në rastin e treguesve të temperaturës së ulët përcaktohet duke përdorur statistikat kuantike. Ekziston parimi Nernst, i cili quhet ligji i tretë i termodinamikës. Bazuar në formulimin e tij, kapaciteti termik molar i një gazi do të ulet me uljen e temperaturës, duke u prirur në zero.

Veçoritë e trupave të ngurtë
Nëse kapaciteti i nxehtësisë i një përzierjeje gazesh mund të shpjegohet duke përdorur statistikat kuantike, atëherë për një gjendje të ngurtë grumbullimi, lëvizja termike karakterizohet nga luhatje të lehta të grimcave pranë pozicionit të ekuilibrit.
Çdo atom ka tre shkallë lirie vibruese, prandaj, në përputhje me ligjin e barazisë, kapaciteti molar i nxehtësisë së një trupi të ngurtë mund të llogaritet si 3nR, ku n është numri i atomeve në një molekulë.
Në praktikë, ky numër është kufiri në të cilin priret kapaciteti i nxehtësisë së një trupi të ngurtë në temperatura të larta.
Maksimumi mund të merret në temperatura të zakonshme për disa elementë, përfshirë metalet. Për n=1, ligji Dulong dhe Petit përmbushet, por për substancat komplekse është mjaft e vështirë të arrihet një kufi i tillë. Meqenëse kufiri nuk mund të arrihet në realitet, ndodh dekompozimi ose shkrirja e lëndës së ngurtë.
Historia e teorisë kuantike
Themeluesit e teorisë kuantike janë Ajnshtajni dhe Deby në fillim të shekullit të njëzetë. Ai bazohet në kuantizimin e lëvizjeve osciluese të atomeve në një të caktuarKristal. Në rastin e treguesve të temperaturës së ulët, kapaciteti termik i një trupi të ngurtë rezulton të jetë drejtpërdrejt proporcional me vlerën absolute të marrë në kub. Kjo marrëdhënie është quajtur ligji i Debye. Si kriter që bën të mundur dallimin ndërmjet treguesve të temperaturës së ulët dhe të lartë merret krahasimi i tyre me temperaturën Debye.
Kjo vlerë përcaktohet nga spektri i dridhjeve të një atomi në trup, prandaj varet seriozisht nga veçoritë e strukturës së tij kristalore.
QD është një vlerë që ka disa qindra K, por, për shembull, është shumë më e lartë në diamant.
Elektronet e përcjelljes japin një kontribut të rëndësishëm në kapacitetin e nxehtësisë së metaleve. Për ta llogaritur atë, përdoren statistikat kuantike Fermi. Përçueshmëria elektronike për atomet metalike është drejtpërdrejt proporcionale me temperaturën absolute. Meqenëse është një vlerë e parëndësishme, ajo merret parasysh vetëm në temperaturat që priren në zero absolute.
Metodat për përcaktimin e kapacitetit të nxehtësisë
Metoda kryesore eksperimentale është kalorimetria. Për të kryer një llogaritje teorike të kapacitetit të nxehtësisë, përdoret termodinamika statistikore. Është e vlefshme për një gaz ideal, si dhe për trupat kristalorë, kryhet në bazë të të dhënave eksperimentale mbi strukturën e materies.
Metodat empirike për llogaritjen e kapacitetit të nxehtësisë së një gazi ideal bazohen në idenë e strukturës kimike, kontributin e grupeve individuale të atomeve në Ср.
Për lëngjet përdoren edhe metoda që bazohen në përdorimin e termodinamikësciklet që bëjnë të mundur kalimin nga kapaciteti termik i një gazi ideal në një lëng përmes derivatit të temperaturës së entalpisë së procesit të avullimit.
Në rastin e një zgjidhjeje, llogaritja e kapacitetit të nxehtësisë si funksion shtesë nuk lejohet, pasi vlera e tepërt e kapacitetit të nxehtësisë së tretësirës është në thelb domethënëse.
Për ta vlerësuar atë, na duhet teoria molekulare-statistikore e zgjidhjeve. Më e vështira është identifikimi i kapacitetit termik të sistemeve heterogjene në analizën termodinamike.

Përfundim
Studimi i kapacitetit të nxehtësisë ju lejon të llogaritni bilancin e energjisë të proceseve që ndodhin në reaktorët kimikë, si dhe në aparatet e tjera të prodhimit kimik. Përveç kësaj, kjo vlerë është e nevojshme për zgjedhjen e llojeve optimale të ftohësve.
Për momentin, përcaktimi eksperimental i kapacitetit të nxehtësisë së substancave për intervale të ndryshme të temperaturës - nga vlerat e ulëta në vlerat e larta - është opsioni kryesor për përcaktimin e karakteristikave termodinamike të një substance. Kur llogaritet entropia dhe entalpia e një substance, përdoren integrale të kapacitetit të nxehtësisë. Informacioni në lidhje me kapacitetin termik të reagentëve kimikë në një gamë të caktuar të temperaturës ju lejon të llogaritni efektin termik të procesit. Informacioni mbi kapacitetin termik të tretësirave bën të mundur llogaritjen e parametrave të tyre termodinamikë në çdo vlerë të temperaturës brenda intervalit të analizuar.
Për shembull, një lëng karakterizohet nga shpenzimi i një pjese të nxehtësisë për të ndryshuar vlerën e energjisë potencialemolekulat reaguese. Kjo vlerë quhet kapaciteti termik i "konfigurimit", i përdorur për të përshkruar zgjidhjet.
Është e vështirë të kryhen llogaritje të plota matematikore pa marrë parasysh karakteristikat termodinamike të një substance, gjendjen e saj të grumbullimit. Kjo është arsyeja pse për lëngjet, gazet, lëndët e ngurta përdoret një karakteristikë e tillë si kapaciteti specifik i nxehtësisë, i cili bën të mundur karakterizimin e parametrave të energjisë së një substance.






